消防設備電源監控系統在防火門電氣信號裝置中的應用探討

消防設備電源監控系統(Fire Equipment Power Supply Monitoring System, FPSMS)是一種專門用于實時監控消防設備供電狀態的關鍵設施,其核心功能是確保消防設備在火災發生時能夠獲得可靠、不間斷的電力供應。隨著智能消防技術的發展,其應用范圍正逐步擴大。該系統是否可以應用于防火門及其相關的電氣信號設備裝置上呢?答案是肯定的,并且這種應用具有重要的現實意義和顯著的技術優勢。
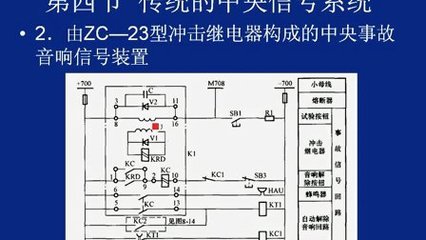
從功能兼容性來看,現代防火門系統,尤其是常開式防火門、電動防火門以及與之聯動的防火門監控系統,都依賴于電力驅動和控制。這些防火門的開啟、關閉、狀態反饋(如常開、常閉、故障)以及與其他消防系統(如火災報警系統)的聯動,都需要通過電氣信號設備裝置來實現。這些電氣裝置,包括電磁釋放器、門磁開關、電動閉門器、控制模塊等,其正常工作離不開穩定、可靠的電源。消防設備電源監控系統正是為了保障這類關鍵消防設備電源的“健康”而設計的。通過將防火門控制箱的供電回路接入FPSMS,可以實時監測其主電和備電的電壓、電流狀態,一旦出現電源過壓、欠壓、缺相、斷電或中斷等故障,監控主機能立即發出聲光報警,并精確定位故障點,提醒維護人員及時處理,從而確保防火門系統在任何時候都處于備戰狀態。
從規范和標準角度分析,國家標準《GB 25506-2010消防控制室通用技術要求》和《GB 29364-2012 防火門監控器》等,均強調了消防設備電源監控的重要性。雖然標準未強制規定所有防火門必須接入FPSMS,但對于設置在消防控制室集中監控、且對供電連續性要求極高的防火門系統(尤其是作為疏散通道關鍵環節的防火門),采用電源監控是提升系統整體可靠性的最佳實踐和未來趨勢。它符合“預防為主,防消結合”的消防工作方針,是對消防設施進行智能化、精細化管理的體現。
從系統集成與聯動層面,將防火門電源監控納入FPSMS,能夠實現更高層次的系統集成。在大型建筑綜合體或智能化建筑中,FPSMS通常作為消防設備電源的“總管家”,可以統一監控包括防火門控制器、應急照明、消防水泵、防排煙風機、火災報警控制器等在內的所有消防設備電源。這樣,當FPSMS監測到為某區域防火門供電的線路出現異常時,不僅可以報警,還可以將此信息上傳至更高層的建筑設備管理系統或消防控制室圖形顯示裝置,為管理人員提供全面的電源健康畫像,便于統籌維護和應急決策。
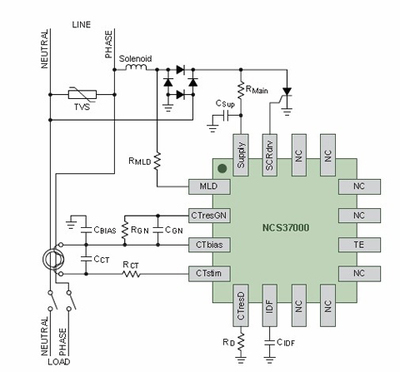
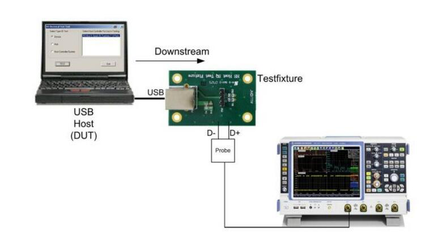
在電氣信號設備裝置的制造環節,這一應用也提出了明確的技術要求。制造商在設計防火門監控模塊、控制箱等電氣信號裝置時,應充分考慮與消防設備電源監控系統的接口兼容性。例如,提供標準的無源干接點故障輸出信號接口,以便于FPSMS的傳感器(電壓/電流信號傳感器)采集其電源狀態。裝置自身的電源設計也應更加穩定、高效,具備良好的抗干擾能力,以適應監控系統的高精度監測需求。
消防設備電源監控系統完全可以且應當應用于防火門及其電氣信號設備裝置上。這種應用通過技術手段,為防火門這一重要的被動防火設施加上了“電源保險”,極大地增強了其在火災中的可靠性和有效性,是構建完善、智能、可靠的現代化消防體系的重要組成部分。對于電氣信號設備裝置制造商而言,這也意味著產品需要向更高標準的可靠性、可監測性和系統集成性方向發展。
如若轉載,請注明出處:http://www.guijiaoxiang.cn/product/51.html
更新時間:2026-05-24 21:10:43